
Per utilizzare questa funzionalità di condivisione sui social network è necessario accettare i cookie della categoria 'Marketing'.
Come migliorare la sicurezza nella diagnostica e nella terapia medico-nucleare

Roma, 19 Mag – Come ricordato nel documento “ Progettazione di ambienti dedicati alla manipolazione di sorgenti non sigillate e alla produzione di radiofarmaci”, realizzato nel 2022 dal Dipartimento di medicina, epidemiologia, igiene del lavoro e ambientale (DIMEILA) dell’ Inail, in ambito sanitario si sta diffondendo l’utilizzo di radionuclidi per le applicazioni di Medicina nucleare (MN). Si tratta di quelle attività che riguardano la produzione e l’utilizzo di sorgenti sigillate e/o non sigillate a scopo medico, sia diagnostico che terapeutico”. Sorgenti che, tuttavia, devono essere “approcciate, da un punto di vista radioprotezionistico, conformemente sia alle buone prassi applicabili, sia alle disposizioni normative vigenti”. Ad esempio con riferimento al d.lgs. 101/2020 relativamente alla protezione contro i pericoli derivanti dall'esposizione alle radiazioni ionizzanti.
Se nei mesi passati, presentando il documento, abbiamo accennato alla diagnostica PET (Positron Emission Tomography) e alla produzione di radiofarmaci con ciclotrone, parliamo oggi dell’utilizzo di radiofarmaci nella medicina nucleare, che ha sicuramente cambiato la diagnosi e la terapia di numerose patologie e con riferimento anche alle prassi per garantire la sicurezza del personale sanitario e la protezione dei pazienti.
Ci soffermiamo oggi sui seguenti argomenti:
- La sicurezza nella medicina nucleare: la terapia medico-nucleare
- La sicurezza nella medicina nucleare: la diagnostica medico-nucleare
- La sicurezza nella medicina nucleare: l’analisi e la limitazione dei rischi
La sicurezza nella medicina nucleare: la terapia medico-nucleare
Un capitolo è dedicato alla terapia medico-nucleare (o radiometabolica) il cui scopo è quello di ottenere un “adeguato controllo della malattia tramite somministrazione di radiofarmaci, sfruttando quindi la mortalità cellulare a seguito di interazione con radiazioni ionizzanti”. E “le patologie più frequentemente trattate sono quelle di origine neoplastica. Vi sono anche applicazioni per patologie benigne, quali ad esempio le forme di ipertiroidismo non più controllabili farmacologicamente”.
Si ricorda che a differenza della diagnostica medico-nucleare, “dove i radionuclidi usati emettono radiazione gamma di energia adeguata per effettuare imaging scintigrafico, in terapia medico-nucleare i radionuclidi impiegati emettono radiazione β- o α, ovvero radiazioni a breve range di penetrazione che irradiano selettivamente gli organi/tessuti in cui si è maggiormente accumulato il farmaco (ovvero, il bersaglio del trattamento), riducendo invece i rischi derivanti dalla esposizione di tessuti o organi sani”. E un’altra differenza fondamentale consiste nelle “attività somministrate che sono molto più elevate rispetto a quelle tipicamente utilizzate in diagnostica, arrivando ad essere fino a circa 100 volte superiori”.
E di conseguenza:
- “qualora il radionuclide usato per terapia emettesse (oltre alla radiazione β- o α) anche radiazione X e γ, i livelli di esposizione esterna dei lavoratori e della popolazione dovuti ad interazioni con il paziente somministrato potrebbero essere molto più elevati rispetto alle attività diagnostiche, dipendentemente anche da abbondanza ed energia della radiazione fotonica emessa”;
- nel caso, ad esempio, di radionuclidi emettitori β- puri, “malgrado l’attività somministrata sia ben più elevata rispetto alle applicazioni diagnostiche, il livello di esposizione esterna causato dal paziente somministrato rimane comunque modesto, o molto limitato, essendo dovuto alla radiazione di frenamento prodotta dall’interazione degli elettroni con i tessuti attraversati e ai pochi elettroni che fuoriescono dal corpo”.
Il documento, che si sofferma poi su alcuni radiofarmaci, indica che poiché le attività somministrate in terapia medico-nucleare “possono essere elevate, il paziente spesso rappresenta una fonte di esposizione e di contaminazione che deve essere opportunamente gestita dal punto di vista radioprotezionistico”. E dipendentemente dal radioisotopo utilizzato e dall’attività somministrata “può rendersi necessario ricoverare il paziente in una degenza protetta”.
Ad esempio, il ricovero in una degenza protetta “con raccolta delle deiezioni dei pazienti è obbligatorio nel caso di somministrazione di 131I in attività superiore a 600 MBq”. E negli altri casi, in seguito all’entrata in vigore del d.lgs. 101/2020, “la necessità di ricovero in una degenza protetta ed eventuale raccolta delle deiezioni deve essere valutata su base individuale, avendo anche in questo caso come obiettivo il rispetto dei vincoli di dose precedenti”.
A questo proposito rimandiamo alla lettura integrale del documento Inail che riporta informazioni di base sulla “gestione delle attività e del paziente, per le modalità terapeutiche più comunemente praticate” e le indicazioni connesse alle possibili esposizioni e rischi.
A titolo esemplificativo indichiamo che “i trattamenti con 131I del carcinoma tiroideo differenziato sono la tipologia di trattamento più frequente ed al tempo stesso quella che presenta i maggiori rischi (Icrp 94, 2004). L’attività somministrata si aggira nell’intervallo 2 - 4 GBq nel caso di ablazione post-intervento del residuo chirurgico, e nell’intervallo 5 - 10 GBq per pazienti a rischio clinico più elevato (malattia recidivante, metastasi locoregionali, o distanti). La somministrazione avviene prevalentemente per via orale e la principale via di eliminazione è quella urinaria, con conseguente elevato livello di contaminazione in caso di vomito o spargimento di urine. Per trattamenti pediatrici, si preferisce somministrare per via endovenosa, per limitare l’esposizione dell’esofago e del tratto gastrointestinale. La buona idratazione dei pazienti è fondamentale per ridurre l’esposizione dei reni e della vescica. L’interazione diretta con i pazienti somministrati deve essere breve e limitata allo stretto indispensabile, e pertanto si prevedono di preferenza dispositivi di comunicazione interfono con le sale di degenza. È opportuno prevedere delle procedure di valutazione che garantiscano il rispetto dei vincoli di dose, come previsto dalla legge”.
La sicurezza nella medicina nucleare: la diagnostica medico-nucleare
Veniamo alla diagnostica medico-nucleare convenzionale.
Si indica che la scelta dei “radionuclidi utilizzati nelle pratiche di diagnostica medico-nucleare convenzionale e delle molecole con funzioni biologiche di trasporto (carrier) nei tessuti dell’organo che si intende studiare è dettata da valutazioni di ordine radiobiologico, tecnico e biochimico, nel rispetto del principio di ottimizzazione (teso ad ottenere il massimo rapporto fra la capacità dell’indagine a risolvere il quesito diagnostico ed il detrimento sanitario cui si sottopone il paziente a causa degli effetti nocivi delle radiazioni ionizzanti)”.
Anche in questo caso il documento fa un approfondimento tecnico, dal punto di vista radiobiologico, su come “minimizzare i contributi di esposizione alle radiazioni non necessarie per l’imaging (quindi diverse da radiazioni γ)”. E indica quali siano i possibili radionuclidi da scegliere così da “minimizzare il contributo di esposizione dovuto all’emissione di elettroni”.
Riprendiamo dal documento una tabella comprendente i radionuclidi più utilizzati in medicina nucleare convenzionale (MNC) con indicazione delle principali proprietà fisiche (tempo di dimezzamento e decadimenti principali):
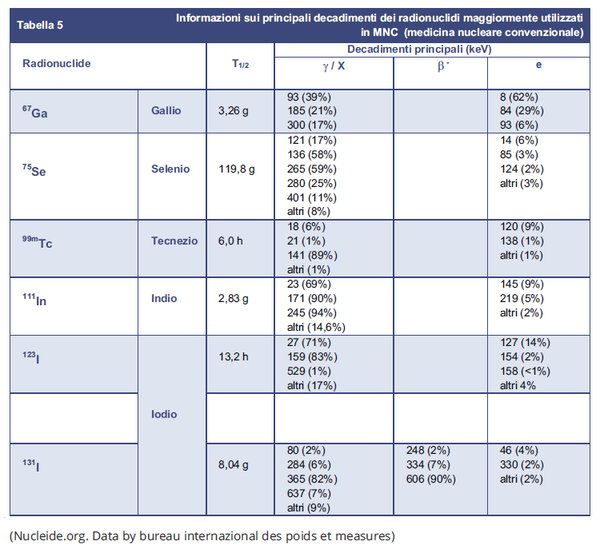
Si ricorda poi che il 99mTc risulta il radionuclide più utilizzato nella diagnostica medico nucleare: ad oggi (alla data di elaborazione del documento) “oltre il 90% degli esami MNC sono effettuati con questo radionuclide”.
Il documento indica poi che, in generale, tutti i radionuclidi elencati sono “caratterizzati da:
- emissioni gamma pure ad esclusione del 59Fe (il cui impiego è limitato ad esami diagnostici molto specifici) e dello 131I (radionuclide di elezione per la diagnosi delle patologie tiroidee, ma sostituibile, in molti casi, con lo 123I o con il 99mTc);
- energie dei gamma emessi normalmente comprese fra i 100 keV ed i 300 keV”.
La sicurezza nella medicina nucleare: l’analisi e la limitazione dei rischi
Veniamo, dunque, all’analisi dei rischi legati all’esercizio della pratica di Medicina nucleare (MN) che, secondo gli autori, è “sintetizzabile come segue:
- rischi da contaminazione delle superfici e delle persone, trattandosi di pratica in cui si impiegano sostanze radioattive non sigillate (trascurabili, normalmente, i rischi da contaminazione dell’aria);
- rischi da irraggiamento, dovuti alle emissioni gamma (come visto, di bassa e media energia) dei radionuclidi utilizzati e delle radiazioni X generate dalle apparecchiature ibride SPECT/CT;
- presenza di sorgenti sigillate, normalmente di bassa attività, utilizzate per il controllo di qualità dei calibratori di dose, delle apparecchiature per imaging e della strumentazione dell’UO di MN, come marker anatomici da posizionare sul paziente;
- rischi da irraggiamento e contaminazione da parte dei pazienti ai quali è stato somministrato il radiofarmaco e diventati per questo essi stessi sorgenti radioattive”.
Concludiamo riportando, invece, alcune indicazioni sulla riduzione dei rischi.
Si indica che la limitazione di tali rischi si ottiene “con l’applicazione dei seguenti principi di base:
- disposizione dei locali strutturata in modo che sia facilitata la corretta applicazione delle logiche di percorso preventivamente definite, passando progressivamente da zone fredde a zone calde, predisponendo un locale di controllo della contaminazione (zona filtro);
- superfici ambientali che siano rivestite con materiali che ne permettano l’adeguata igienizzazione, garantendo una resistenza agli agenti chimici e al contempo una facilità di decontaminazione della superficie stessa;
- presenza di idonee attrezzature per la manipolazione ed il contenimento dei radiofarmaci, delle sorgenti sigillate e dei rifiuti radioattivi;
- idonee schermature per i locali ove sia previsto l’impiego delle sorgenti radioattive e presenza di idonei contenitori schermati per il trasporto delle sorgenti stesse;
- individuazione preventiva delle possibili fonti di rischio potenziale”.
Rimandiamo, in conclusione, alla lettura integrale del documento che riporta molti altri dettagli e si sofferma su diverse attività e strategie radioprotezionistiche con riferimento anche alla normativa vigente.
RTM
Scarica il documento da cui è tratto l'articolo:
Inail, Dipartimento di medicina, epidemiologia, igiene del lavoro e ambientale, “ Progettazione di ambienti dedicati alla manipolazione di sorgenti non sigillate e alla produzione di radiofarmaci”, Indicazioni operative aggiornate e integrate per la conformità al d.lgs. 101/2020, a cura di Maria Antonietta D’Avanzo, Massimo Mattozzi e Francesco Campanella (Inail – Dimeila), Gian Marco Contessa e Sandro Sandri (Enea), Stefano Adamo De Crescenzo (Istituto europeo di oncologia), Luca Indovina (Fondazione Policlinico universitario A. Gemelli IRCCS) e Gian Luca Poli (ASST Papa Giovanni XXIII), Collana Salute e Sicurezza, edizione 2022 (formato PDF, 1.97 MB).
Vai all’area riservata agli abbonati dedicata a “ La progettazione e la sicurezza negli ambienti dedicati alla manipolazione di sorgenti non sigillate e alla produzione di radiofarmaci”.
Scarica la normativa di riferimento:
I contenuti presenti sul sito PuntoSicuro non possono essere utilizzati al fine di addestrare sistemi di intelligenza artificiale.
Per visualizzare questo banner informativo è necessario accettare i cookie della categoria 'Marketing'



